
目的:利用美国食品药品监督管理局公共数据开放项目(OpenFDA)检索并分析盐酸环喷托酯滴眼液药品不良反应(adverse drug reactions,ADRs)的报告情况,为临床安全用药提供参考。 方法: 以“盐酸环喷托酯滴眼液”作为检索词,在OpenFDA数据库中检索2004年1月1日至2024年8月1日期间盐酸环喷托酯滴眼液相关ADRs的所有信息,对检索到的数据进行分析。 结果:共检索到盐酸环喷托酯滴眼液相关ADRs 1185例。1185例患者中,剔除性别不详后,女性和男性分别为516例和483例(43.54% vs 40.76%);剔除年龄不详后,ADRs发生率较高的是65~<80岁患者(221例,18.65%)、50~<65岁患者(176例,14.85%)、3~<13岁患者(140例,11.81%)。盐酸环喷托酯滴眼液发生率较高的ADRs为眼器官疾病(767例,64.73%)、神经系统疾病(254例,21.43%)及胃肠系统疾病(228例,19.24%)。 结论:盐酸环喷托酯滴眼液可发生眼局部和全身ADRs,临床在使用时应详细询问患者疾病史和用药史,加强用药监护,提高患者用药的安全性。
· 盐酸环喷托酯滴眼液可发生眼局部和全身不良反应,发生率较高的不良反应为眼器官疾病、神经系统疾病及胃肠系统疾病。
· 盐酸环喷托酯滴眼液在国外是儿童睫状肌麻痹验光的首选药物,近年在国内应用也越来越多。国外有较多文献报道环喷托酯滴眼后可发生全身性的药物不良反应,但国内对于其安全性的报道较少。本研究以OpenFDA数据库为基础,检索并分析盐酸环喷托酯滴眼液不良反应发生的情况,为临床安全合理用药提供参考。
· 本研究利用OpenFDA数据库,挖掘盐酸环喷托酯滴眼液在真实世界中的不良反应,发现不良反应的发生与患者年龄、基础疾病史、用药浓度及剂量相关,提示临床使用盐酸环喷托酯滴眼液时,应加强监护,提高用药安全性。
环喷托酯是人工合成的毒簟碱型胆碱受体(M胆碱受体)拮抗剂,通过阻断乙酰胆碱在虹膜括约肌和睫状肌上的M受体,产生散瞳和睫状肌麻痹的作用。与阿托品相比,环喷托酯起效快,作用时间短,在国外作为儿童睫状肌麻痹验光的首选药物,近年在国内应用也越来越多[1-5]。随着盐酸环喷托酯滴眼液的广泛使用,其安全性也应引起重视,国外有较多文献报道环喷托酯滴眼后可发生全身性的药物不良反应(adverse drug reactions, ADRs)[6-9],但国内对于其安全性的报道较少。
2014年6月,美国食品药品监督管理局(Food and Drug Administration FDA)启动一项在线健康公共数据公开项目 (OpenFDA),通过该网站的开放应用程序接口 (application programming interface , API),公众可以获得ADRs相关数据[10-14]。该数据库中有自2004年至目前上报的约1 800万份药品不良事件,已成为发现ADRs信号的一个重要数据来源。本研究以OpenFDA数据库为基础,检索并分析盐酸环喷托酯滴眼液ADRs发生的情况,为临床安全合理用药提供参考。
数据源于OpenFDA数据库的检索程序接口API,选择药品不良事件检索端点Drug API Endpoints,选择交互式图表板块Explore the APl with an interactive chart。以“盐酸环喷托酯滴眼液”为目标药品,以“cyclopentolate hydrochloride eye drops”为检索词,在OpenFDA 数据库中检索相关ADRs信息。
收集盐酸环喷托酯滴眼液相关ADRs的数量及上报年份、上报国家、上报人员职业;发生ADRs患者的年龄、性别、职业;相关ADRs的严重程度、累及器官(或系统)及其临床表现、最终转归等信息。检索时间段为2004 年1月1日至2024年8月1日。按照《国际医学用语词典(MedDRA)》中的首选系统器官分类(system organ classification, SOC)和首选术语(preferred term, PT)对ADRs 累及器官或系统及临床表现进行分类,用EXCEL软件对所得数据进行整理分析。
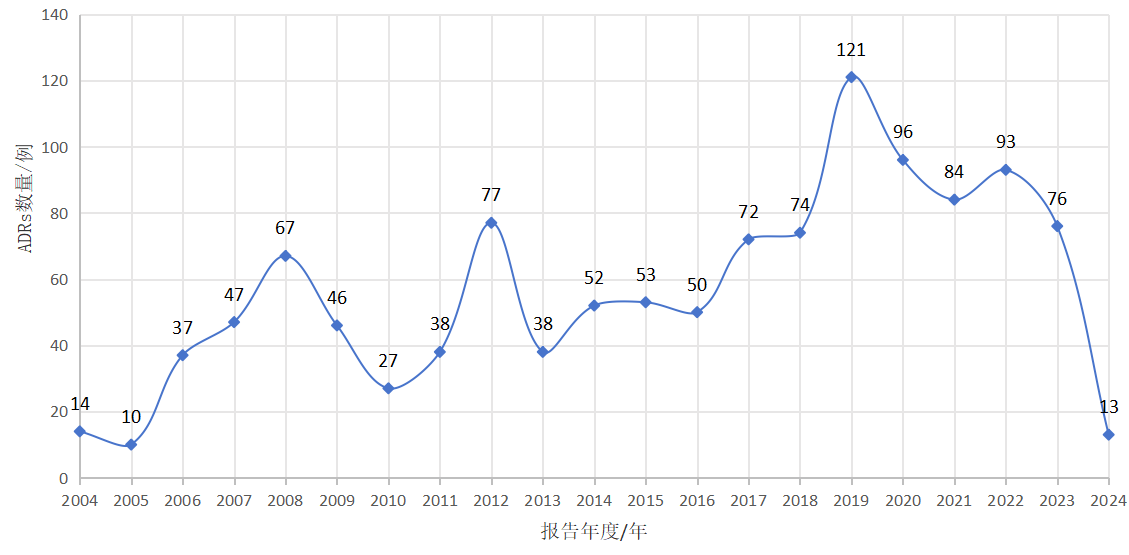
截至 2024年8月1日,在OpenFDA数据库中共检索到盐酸环喷托酯滴眼液相关ADRs 1 185例,自2004年上报14例以后,每年的上报数量呈波动上升趋势,年度上报分布见图1。
在1 185例相关ADRs中,以美国上报的例数最多(461例,38.90%),其次为英国(258 例,21.77%);上报人员主要为医师(235例,19.83%)和其他医务人员(512例,43.21%)。发生 ADRs 的患者中,剔除性别不详后,女性略多于男性( 516例,43.54% vs 483例,40.76%);剔除年龄不详后,ARDs发生率最高的是65~<80岁患者(221例,18.65%),其次是50~<65岁患者(176例,14.85%),和3~<13岁患者(140例,11.81%)。详见表 1。
|
例数 |
构成比/% |
|
|
上报国家(前5位) |
|
|
|
美国 |
461 |
38.90 |
|
英国 |
258 |
21.77 |
|
德国 |
58 |
4.89 |
|
加拿大 |
50 |
4.22 |
|
法国 |
49 |
4.14 |
|
其他 |
309 |
26.08 |
|
上报人员职业 |
|
|
|
其他医务人员 |
512 |
43.21 |
|
医师 |
235 |
19.83 |
|
消费者及非医务人员 |
200 |
16.88 |
|
药师 |
93 |
7.85 |
|
律师 |
10 |
0.84 |
|
不详 |
135 |
11.39 |
|
患者性别 |
|
|
|
女 |
516 |
43.54 |
|
男 |
483 |
40.76 |
|
未知 |
186 |
15.70 |
|
年龄 |
|
|
|
≤2岁 |
13 |
1.10 |
|
3~<13岁 |
140 |
11.81 |
|
13~<18岁 |
26 |
2.19 |
|
18~<35岁 |
70 |
5.91 |
|
35~<50岁 |
77 |
6.50 |
|
50~<65岁 |
176 |
14.85 |
|
65~<80岁 |
221 |
18.65 |
|
≥80岁 |
116 |
9.79 |
|
不详 |
346 |
29.20 |
盐酸环喷托酯滴眼液相关 ADRs 的 SOC的前五位为眼器官疾病(64.73%)、各类神经系统疾病(21.43%)、胃肠系统疾病(19.24%)、全身性疾病及给药部位各种反应(17.64%)、心脏器官疾病(5.32%)。同一患者的ADRs可能涉及2个以上PT,故例次数大于上报总例数,详见表2。
|
SOC |
PT(n/例次) |
例次 |
构成比/% |
|
眼器官疾病 |
中毒性眼前节综合征(82)、虹膜松弛综合征(64)、眼痛(45)、视力模糊(42)、角膜病变(41)、眼内炎(39)、视力下降(39)、瞳孔散大(37)、视力障碍(37)、白内障(36)、眼内压升高(36)、虹膜睫状体炎(30)、失明(28)、视网膜脱离(23)、角膜沉积物(22)等 |
767 |
64.73 |
|
各类神经系统疾病 |
头痛(56)、眩晕(42)、癫痫发作(19)、嗜睡(19)、幻觉(17)、意识丧失(17)、定向障碍(16)、焦虑(15)、感觉异常(14)、言语障碍(14)、平衡失调(9)、健忘症(8)、精神错乱(8) |
254 |
21.43 |
|
胃肠系统疾病
|
恶心(52)、呕吐(40)、腹泻(31)、腹胀(18)、痔疮(12)、便秘(13)、腹部不适(10)、胃食管反流病(11)、胃残余增加(9)、坏死性结肠炎(9)、直肠出血(15)、上腹痛(8) |
228 |
19.24 |
|
全身性疾病及给药部位各种反应 |
疲劳(33)、病情加重(28)、不适(16)、虚弱(11)、疾病进展(10)、疼痛(14)、跌倒(10)、发热(24)、背痛(25)、晕厥(13)、脱发(13)、胸腔积液(12) |
209 |
17.64 |
|
心脏器官疾病 |
心动过缓(24)、心动过速(16)、射血分数下降(12)、循环衰竭(11) |
63 |
5.32 |
|
呼吸系统、胸及纵隔疾病 |
呼吸困难(34)、呼吸暂停(14)、咳嗽(11) |
59 |
4.98 |
|
肾脏及泌尿系统疾病 |
肾功能衰竭(20)、慢性肾病(18)、急性肾损伤(15) |
53 |
4.47 |
|
各类检查 |
高血压(10)、低血压(14)、血氧饱和度降低(10)、C反应蛋白升高(8) |
42 |
3.54 |
|
皮肤及皮下组织类疾病 |
红斑(14)、皮疹(9)、荨麻疹(9) |
32 |
2.70 |
|
各种肌肉骨骼及结缔组织疾病 |
骨质减少(12)、关节痛(11) |
23 |
1.94 |
|
代谢及营养类疾病 |
体质量下降(18) |
18 |
1.52 |
|
各类损伤、中毒及手术并发症 |
术后并发症(17) |
17 |
1.43 |
|
免疫系统疾病 |
超敏反应 13 |
13 |
1.10 |
|
感染及侵染类疾病 |
炎症 13 |
13 |
1.10 |
|
血液与淋巴系统疾病 |
贫血 11 |
11 |
0.93 |
|
合计 |
|
1 802 |
100 |
1 185例发生ADRs的患者转归情况见表3。
|
例次 |
构成比/% |
|
|
未知 |
540 |
45.57 |
|
恢复 |
320 |
27.00 |
|
未恢复 |
139 |
11.73 |
|
好转 |
104 |
8.78 |
|
后遗症 |
58 |
4.89 |
|
致死 |
24 |
2.03 |
|
合计 |
1185 |
100.00 |
盐酸环喷托酯滴眼液相关 ADRs自2004年上报14例以后,每年的上报数量呈波动上升趋势,这与盐酸环喷托酯滴眼液的广泛使用有关系。上报国家主要为欧美国家,在中国及其他国家上报数量较少,这与盐酸环喷托酯滴眼液的药品供应及临床使用情况有关系,但也反映了国内对滴眼液的ADRs关注相对较少。ADRs 报告人群职业分布包括医师、其他医务人员、消费者及非医务人员、药师等,这说明在欧美国家,医务人员和公众发现盐酸环喷托酯滴眼液ADRs后,具有较高的ADRs上报意识,值得国内学习。上报的患者基本信息中,男性患者和女性患者例数差别不大,说明ADRs的发生与性别无关。
盐酸环喷托酯滴眼液药品说明书提示,ADRs在儿童和老年患者中更加频发[15]。目前,国内外的医学研究中对于患者年龄的划分标准不统一[16],笔者参考文献[17]及结合本研究的特点,将患者年龄共划分为8个年龄段。因成年组患者和老年组患者年龄跨度较大、人口基数大,故将成年患者再细分为3组,将老年患者再细分为2组。患者年龄段划分越细,越能反映年龄与ADRs发生的关系。结果发现 65~<80岁、50~<65岁及3~<13岁患者发生ARDs的患者较多。≤2岁和≥80岁患者可能由于患者数量较少,所以上报数量少。本研究发现,盐酸环喷托酯滴眼液ADRs的发生与患者的年龄相关,且与说明书中的提示一致。
3.2.1 眼器官疾病
滴眼液容易发生眼部刺激、过敏等不良反应,主要原因有以下几点:患者自身体质、滴眼液药物本身的理化性质、滴眼液中某些辅料等[18],如防腐剂可引起角膜上皮损害或刺激症状等。盐酸环喷托酯滴眼液中含有抑菌剂苯扎氯铵,苯扎氯铵是季铵盐类表面活性剂,其分子由亲水极和疏水极两部分组成,疏水极可以和角膜的脂质成分结合,导致眼表损伤[19]。另外还有硼酸、依地酸二钠、氯化钾等药用辅料,滴眼后可能会出现烧灼感、结膜充血、结膜炎等不良反应[15,18]。环喷托酯滴眼后,会作用于虹膜括约肌和睫状肌上的M受体,散大瞳孔,产生视近物不清的效果。瞳孔散大时虹膜退向周边,使得虹膜根部增厚、房角变窄,房水流出受阻,引起眼内压升高。虹膜松弛综合征、视力模糊、眼内压升高等ADRs是由于其药理作用导致,与阿托品滴眼液的不良反应相似[20]。
3.2.2 各类神经系统疾病
盐酸环喷托酯滴眼液说明书[15]中明确警告“本品可能会造成任何年龄阶段的患者中枢神经系统障碍,特别是在年龄较小的群体中,及使用高浓度溶液的患者。” 说明书提示神经系统ADRs表现为头晕、嗜睡、定向力障碍、幻觉、共济失调、言语障碍、癫痫发作,与本研究的结果基本一致。国内黄春联等[21]报道过一例6岁儿童使用1%盐酸环喷托酯滴眼液点眼3次后,出现中枢神经系统方面的ADRs,约1 h后,症状减轻并逐渐恢复正常。盐酸环喷托酯滴眼液使用后,可以经鼻泪管到达口腔,进入消化系统,产生全身吸收,引起胆碱能副作用。大脑中有广泛的乙酰胆碱受体,对于焦虑、抑郁、记忆、精神疾病等具有重要的调节作用[22]。使用盐酸环喷托酯滴眼液并产生全身吸收后,中枢胆碱受体被阻断,从而导致了中枢神经系统ADRs。
说明书提示及文献报道的与发生中枢神经系统ADRs相关的因素[7,15,23-24]包括:1)年龄:低龄儿童发生中枢神经系统ADRs的风险比成人高,儿童应谨慎使用盐酸环喷托酯滴眼液,用药后密切观察30 min;2)中枢神经系统疾病病史,使用盐酸环喷托酯滴眼液后更容易发生中枢神经系统ADRs,可能是由于此类患者中枢神经系统对环喷托酯的敏感性较高;3)盐酸环喷托酯滴眼液的浓度与使用剂量,使用高浓度或大剂量时,更易发生中枢神经系统ADRs。婴幼儿不宜使用1%和2%的环喷托酯滴眼,必须用药时,应降低浓度,否则婴幼儿可能会发生痉挛麻痹或脑损害。
3.2.3 其他SOC
M胆碱受体广泛分布于全身的各个器官组织,起到胆碱能神经传递的作用[25]。环喷托酯是人工合成的M胆碱受体阻断药,其滴眼液虽为眼局部使用的药物,但产生全身吸收后可引起一系列的与M受体被阻断的相关ADRs。如作用于胃肠道平滑肌的M受体,可抑制平滑肌痉挛,降低蠕动的幅度和频率,所以会引起腹胀、便秘、腹部不适、胃残余增加等ADRs。如作用于心血管系统的M受体,可引起心率减慢或加快、血管扩张,进而引起血压升高或降低、皮肤潮红等。如作用于唾液腺和汗腺的M受体,可抑制腺体分泌,导致口干和皮肤干燥,且出汗减少影响了机体散热,又导致体温上升。以上ADRs均为环喷托酯的药理作用导致,说明书中均有提及[15]。
对于本研究发现的且说明书未收录的ADRs信号如呼吸困难、呼吸暂停、咳嗽、骨质减少、关节痛、体质量下降、贫血等,尚无相关文献报道。ARDs为“可疑即报”原则,从OpenFDA数据库获得的数据不包含患者的基础疾病及合并用药情况,可能会导致某些ARDs的因果关系存疑,但以上ADRs信号仍对盐酸环喷托酯滴眼液的临床使用有一定的指导意义。
从本研究中盐酸环喷托酯滴眼液 ADRs所涉及患者的转归情况来看,未知结局占比较高,这可能与上报数据不完整有关系。除了未知结局外,恢复和好转占多数,未恢复和后遗症的患者也占相当比例,甚至出现了致死的结局。文献[23 -24, 26]报道盐酸环喷托酯滴眼液的不良反应都是轻微的、短暂的,可以在24 h内自行消退,与本研究结果不一致。考虑到OpenFDA数据库源于公众自发呈报,数据可能存在偏差,但本研究结果仍对临床安全合理用药有警示作用。在使用盐酸环喷托酯滴眼液前,医师应充分了解患者的基础疾病史、用药史等情况,使用时密切观察,发生ARDs时及时干预,避免留下后遗症或出现严重结局。药师也应对患者做好用药教育,指导患者滴眼后闭眼2 min,用手指压迫闭合泪管2 min,以减少全身吸收,尽量规避ADRs的发生[15]。
OpenFDA是公众自发呈报的数据库,上报人员职业及素质的差异可导致上报数据的质量及完整性存在一定程度的偏倚。从OpenFDA数据库中得到的数据只有结果信息,无法准确了解患者的合并用药、用药疗程及剂量等情况,不能确证药物与上报的ADRs的因果关系。上报的数据主要来源于欧美国家,由于存在种族差异、地区差异等,盐酸环喷托酯滴眼液在中国人群中ADRs的发生情况有待进一步的追踪。但OpenFDA数据库可以提供不同国家不同人群的、大样本量的真实数据,是发掘ADRs的宝贵资源,如本研究发现盐酸环喷托酯滴眼液眼局部使用后,中枢神经系统ADRs占比较高,提示用药时应加强监护。
综上所述,本研究利用OpenFDA数据库,挖掘盐酸环喷托酯滴眼液在真实世界中的ADRs,发现盐酸环喷托酯滴眼液发生率高的ADRs与说明书提示一致,为眼器官疾病和中枢神经系统疾病,说明书未收录的ADRs也应引起临床医师的关注。盐酸环喷托酯滴眼液ADRs的发生与患者年龄、基础疾病、用药浓度及剂量相关,临床使用时应加强监护,提高患者用药的安全性。
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。


点击右上角菜单,浏览器打开下载